Đột phá mới: Thiết bị cầm tay giúp mẹ bầu tự siêu âm tại nhà
Đây là lần đầu tiên một thiết bị siêu âm được FDA cho phép sử dụng tại nhà, không yêu cầu người dùng phải có chuyên môn y tế.
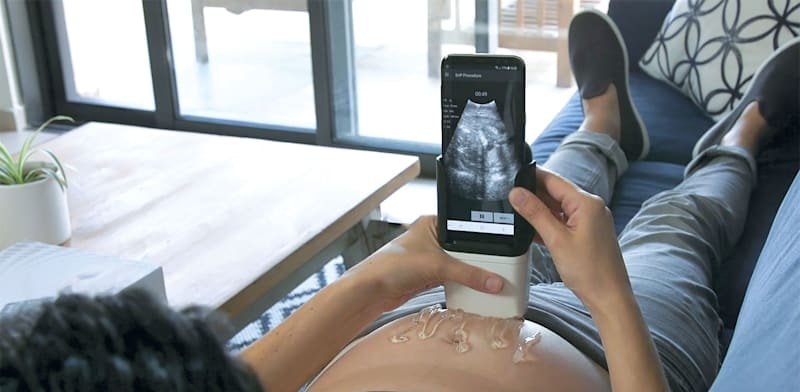
Một thiết bị siêu âm cầm tay cho phép phụ nữ mang thai tự thực hiện siêu âm tại nhà vừa chính thức được Cục Quản lý Thực phẩm và Dược phẩm Mỹ phê duyệt.
Thiết bị do công ty công nghệ y tế Israel Pulsenmore phát triển, đánh dấu một cột mốc mới trong lĩnh vực chăm sóc thai sản và y học từ xa.
FDA lần đầu cấp phép cho thiết bị siêu âm dùng tại nhà
Theo bài viết đăng trên Globes, FDA Mỹ đã cấp phép lưu hành cho thiết bị siêu âm thai tại nhà của Pulsenmore theo diện De Novo 510(k). Đây là con đường phê duyệt dành cho những thiết bị y tế hoàn toàn mới, chưa từng có tiền lệ trên thị trường Mỹ.
Đáng chú ý, trong nhãn hướng dẫn chính thức, FDA nêu rõ thiết bị được thiết kế cho sử dụng tại nhà. Thai phụ có thể dùng thiết bị với sự hỗ trợ chuyên môn từ xa của nhân viên y tế, hoặc tự thực hiện siêu âm dựa trên hệ thống hướng dẫn số tích hợp trong ứng dụng, ngay cả khi không có chuyên gia trực tiếp theo dõi.
Theo Pulsenmore, đây là lần đầu tiên FDA cấp phép cho một thiết bị siêu âm với phạm vi sử dụng như vậy.
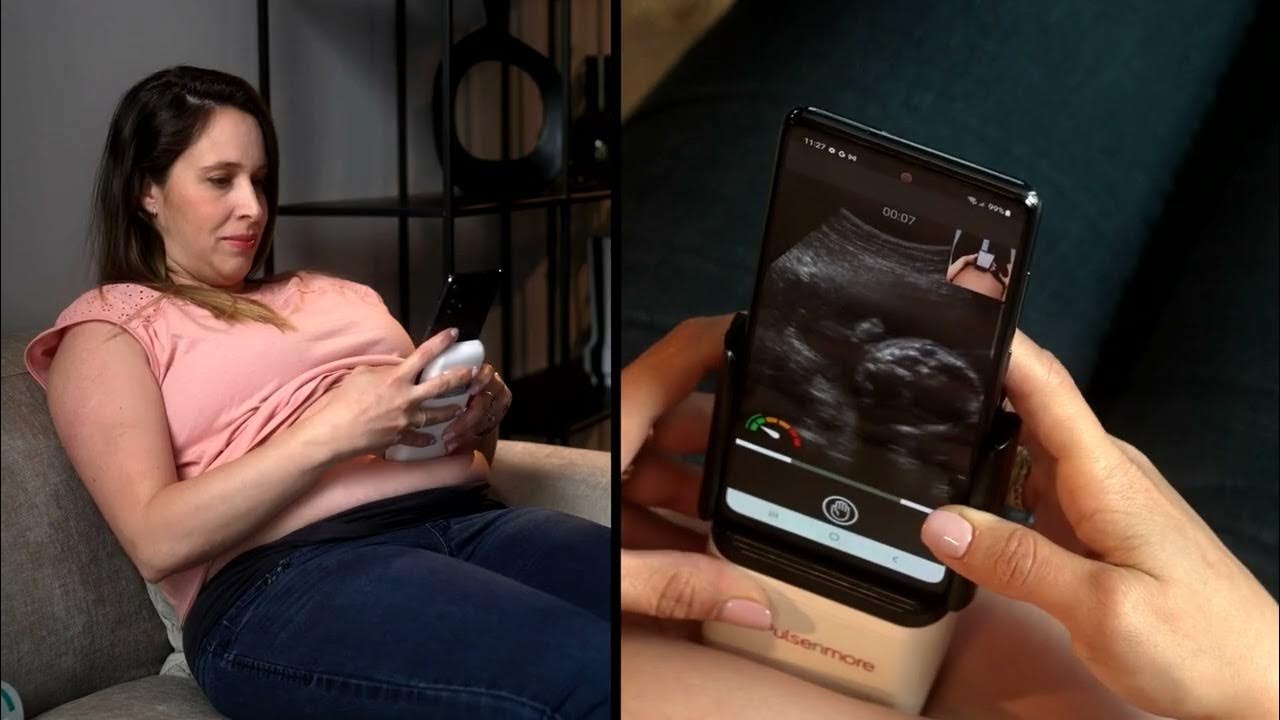
Cách thiết bị hoạt động
Thiết bị siêu âm của Pulsenmore có kích thước nhỏ gọn, kết nối với điện thoại thông minh thông qua một ứng dụng chuyên dụng. Ứng dụng này hướng dẫn người dùng từng bước trong quá trình quét siêu âm, giúp đảm bảo thao tác đúng và an toàn.
Trong những trường hợp cần thiết, dữ liệu siêu âm có thể được chia sẻ để bác sĩ theo dõi từ xa và đưa ra hướng dẫn bổ sung. Thiết kế này nhằm hỗ trợ thai phụ theo dõi thai kỳ giữa các lần khám trực tiếp tại cơ sở y tế.

Trước khi được FDA phê duyệt, Pulsenmore đã triển khai thiết bị tại Israel thông qua hợp tác với Clalit Health Services, một trong những tổ chức chăm sóc sức khỏe lớn nhất nước này.
Theo CEO Pulsenmore, tiến trình xin phê duyệt tại Mỹ kéo dài hơn dự kiến do các thử nghiệm lâm sàng bị chậm lại sau khi đại dịch Covid 19 kết thúc. Trước đó, công ty từng ký thỏa thuận hợp tác chiến lược với GE Healthcare, nhưng thỏa thuận này đã chấm dứt khi Pulsenmore chưa thể đạt được phê duyệt FDA trong thời gian mong muốn.
Sau khi được cấp phép, Pulsenmore cho biết sẽ chuẩn bị đưa sản phẩm ra thị trường Mỹ, đồng thời cân nhắc hợp tác với các đối tác phân phối phù hợp.
Một bước tiến mới của y học từ xa trong thai sản
Việc FDA phê duyệt thiết bị siêu âm dùng tại nhà được xem là bước tiến đáng chú ý của y học từ xa, đặc biệt trong lĩnh vực chăm sóc thai kỳ.
Tuy nhiên, các chuyên gia cũng nhấn mạnh rằng thiết bị này không thay thế hoàn toàn các buổi khám thai định kỳ, mà đóng vai trò hỗ trợ theo dõi, giúp thai phụ an tâm hơn giữa các lần thăm khám trực tiếp.
Trong bối cảnh công nghệ y tế ngày càng cá nhân hóa và dịch chuyển về phía người dùng, sự xuất hiện của thiết bị siêu âm tại nhà được FDA công nhận cho thấy cách chăm sóc thai sản trong tương lai có thể sẽ linh hoạt hơn, nhưng vẫn cần được đặt dưới sự giám sát y khoa phù hợp.
*Nội dung bài viết được biên soạn nhằm mục đích cung cấp thông tin sức khỏe hữu ích, không thay thế cho chẩn đoán hay điều trị y khoa. Nếu bạn có vấn đề về sức khỏe, hãy tham khảo ý kiến bác sĩ chuyên khoa.